Le Nuove Frontiere della Medicina | Analisi Genetica e Medicina Personalizzata

“Ogni essere umano è speciale a modo suo” – questa banale verità, forse un pò troppo zuccherosa per essere vera, sta spianando la via alle nuove frontiere della medicina.
Gli esseri umani infatti sono tutti diversi, ma l’unica differenza a contare in campo medico, è percepibile soltanto al microscopio. La nuova rotta tracciata dalla medicina moderna punta ad una sempre maggiore personalizzazione delle cure.
Parliamo della cosiddetta ‘medicina di precisione’ o medicina personalizzata.
Ma per essere effettivamente “precisa” e garantire un trattamento individualizzato a 360° gradi, la medicina personalizzata deve tenere traccia sia del corredo genetico sia delle influenze ambientali in grado di incidere sulla salute umana.
Si tratta di un obiettivo senz’altro ambizioso – vediamo di capire a che punto siamo!
Le Differenze Contano: DNA e Polimorfismo Genetico
Il polimorfismo genetico è un termine complesso che sta a indicare una variazione davvero minima del proprio codice genetico, la quale, tuttavia, può fare una differenza davvero enorme. La presenza di una mutazione genetica, apparentemente molto piccola, (una sostituzione, un’inserzione o una delezione di una delle basi che formano il DNA), può determinare, infatti, il successo di una specifica terapia farmacologica, la comparsa (o meno) di effetti collaterali o persino la probabilità di contrarre una certa malattia.
Ricordiamoci che il DNA, è il “codice della vita”, un libretto delle istruzioni, necessario a creare gli esseri viventi. Ognuno di noi infatti, è una sorta di gigantesca costruzione Lego, in cui ogni blocco è costituito da una sequenza di basi, o nucleotidi (le quattro basi sono l’adenina(A), la citosina(C), la guanina(G) e la timina(T)) combinati tra loro in modi diversi.
Come spiega Riccardo Sabatini, scienziato e imprenditore nel suo brillante discorso su TedEd, leggendo il codice genetico del cromosoma 14: “ATT, CTT, GAT – questo essere umano è fortunato, perché se gli mancassero solo due lettere in questo punto – due lettere su 3 miliardi – sarebbe condannato alla fibrosi cistica”.
Guarda il video intregale sottotitolato in italiano:
La mappatura del genoma umano, completata nel 2003 dal Human Genome Project, ha dato una forma tangibile al sogno della medicina moderna. A provarlo sono diverse campagne di sponsorizzazione delle ricerche nel campo della medicina personalizzata, tra le quali spicca quella lanciata da Obama nel 2015, la “National Precision Medicine Initiative”, mentre in Europa, nel 2012, è stata formata la European Alliance for Personalised Medicine (EAPM), con l’obiettivo di promuovere la ricerca e l’attuazione di politiche sanitarie da parte del Parlamento Europeo, volte al sostegno della personalizzazione delle cure mediche.
La Farmacogenetica: Stessa Malattia, Farmaci Diversi
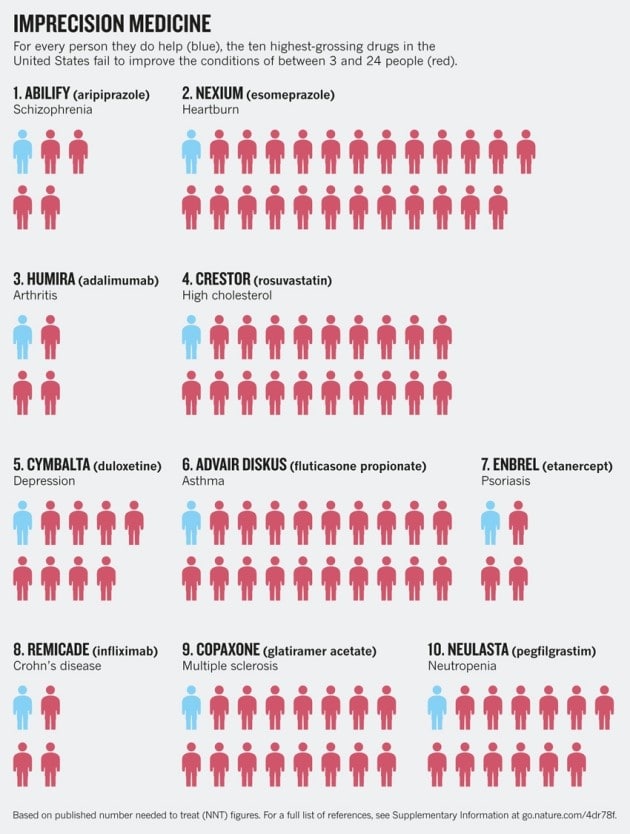
Il primo importante campo di applicazione della precision medicine, riguarda la prescrizione dei farmaci. Le terapie farmacologiche attuali sono state definite in un articolo comparso sulla rivista Nature, come ‘Medicina dell’Imprecisione’. Questo perché i farmaci funzionano anche in base alla presenza o meno di determinate mutazioni genetiche. Secondo un’indagine condotta negli Stati Uniti, milioni di persone, tutti i giorni, assumono farmaci, senza sapere che quelli più venduti funzionano solo per una persona su 4, nella migliore delle ipotesi. Le statine, per esempio, abitualmente usate per abbassare il colesterolo, possono beneficiare una persona su 50! Esistono, poi, farmaci persino dannosi per alcuni gruppi etnici, un dato spesso trascurato in fase di sperimentazione.
La speranza della farmacogenetica è quella di poter prevedere in anticipo gli effetti di un dato farmaco, grazie ad un’analisi genetica preliminare. Leggi: Monografia “I farmaci oncologici associati a test genetico-molecolari”-2015-Centro Studi e Ricerche sulle Biotecnologie Sanitarie e Settore Biotech.
Oggi ci sono diversi farmaci per cui è possibile effettuare un test genetico pre-trattamento. Per alcuni farmaci oncologici il test genetico è stato reso obbligatorio dalla European Medicines Agency (EMA)Clicca per leggere le linee guida per l’utilizzo delle metodologie farmacogenomiche nella valutazione dell’efficacia dei farmaci.
Consulta l’elenco dei farmaci per i quali esistono dei marcatori genetici, con indicazioni su dosaggi e analisi genetiche da effettuare prima del loro utilizzo, visitando il sito di PharmGKB .
Analisi Genetica – A Che Punto Siamo Oggi?
Vi ricordate Minority Report? Il futuristico film con protagonista Tom Cruise, dove il riconoscimento genetico (tramite scannerizzazione degli occhi), consente di entrare nel proprio ufficio, aprire la macchina, ma anche vedere apparire enormi pubblicità, altamente personalizzate e che sembrano conoscerti da sempre. Il crescente interesse globale per il DNA ci sta avvicinando sempre di più a questa realtà fantascientifica.
Come riassume in modo puntuale il programma Report Clicca per vedere la puntata Il Patrimonio, bisogna fare attenzione nella scelta dell’azienda alla quale rivolgersi per ottenere il profilo della propria identità genetica, dato che, come è successo nel caso della 23andMe, si rischia di svendere il proprio patrimonio genetico, in cambio di un’analisi approssimativa e di incerta utilità personale. La FDA (Federal Drug Administration) ha, infatti, richiesto che l’azienda ritiri le proprie campagne di marketing e sospenda la vendita dei servizi di analisi genetica orientata alla storia di malattia, dato che non raggiunge gli standard ritenuti necessari per eseguire questo tipo di procedura.
Già ad oggi i colossi dell’internet possiedono un dossier abbastanza dettagliato sui nostri gusti, interessi e preferenze (grazie alle più avanzate tecniche di profilazione), ma ricordiamoci che se ci vengono proposti cibi, creme o persino partner di vita, scelti in base all’assetto genetico, si tratta solo di speculazione!
É indubbiamente entusiasmante la prospettiva di un approccio medico perfezionato su misura, ma non facciamo il passo più lungo della gamba. Consideriamo che:
- I fattori genetici che influenzano la risposta ad un farmaco sono complessi e non tutti identificabili a priori. La relazione Gene X – Processo Y, non è una relazione lineare.
-
L’eredità genetica non è il destino. Possiamo ottenere soltanto delle stime circa il rischio di contrarre una data malattia. Inoltre, come spiega Marco Pierotti, direttore scientifico dell’Istituto Nazionale Tumori di Milano, il 90-95% delle alterazioni dei geni avviene durante la vita adulta delle cellule, dunque la maggior parte delle trasformazioni non è ereditabile né trasmissibile.
- Se è vero che la medicina ha identificato alcuni geni che aumentano la predisposizione ad ammalarsi di determinate malattie, è anche vero che cercarli è utile solo in casi selezionati. Consulta un genetista esperto per sapere se ci sono indicazioni al test genetico.
Test Genetici e Centri Specializzati
Perchè Fare il Test Genetico?
- Le analisi genetiche consentono di ottenere un quadro personalizzato della propria ereditarietà genetica sia rispetto ad alcune malattie (per la presenza di specifiche mutazioni), sia rispetto alla presenza di determinati fattori di rischio per la salute. I test genetici di questo tipo, non sono da considerare alla stregua di una diagnosi medica, ma rappresentano una modalità accessibile per coltivare un atteggiamento consapevole circa la propria salute.
- Per eseguire il test è necessario prenotare una consulenza genetica presso una struttura specializzata.
Quando Fare il Test Genetico?
Per capire se occorre fare un test del DNA per conoscere l’eventuale presenza di un alto rischio di contrarre un determinato tipo di tumore, secondo l’Istituto Europeo di Oncologia, ci sono cinque domande a cui rispondere:
– Lei o un suo parente prossimo avete avuto una diagnosi di tumore in giovane età?
– Qualche suo parente prossimo ha avuto lo stesso tipo di tumore che ha avuto lei? Se sì lo stesso tipo di tumore è stato riscontrato in più di una generazione?
– A qualcuno della sua famiglia è stato diagnosticato più di un tipo di tumore (Escludendo i tumori della pelle “non melanoma”)?
– Qualcuno della sua famiglia ha avuto un tumore bilaterale negli organi pari, per esempio seno, ovaio?
– In qualcuno della sua famiglia è già stata identificata una mutazione genetica che possa aumentare il rischio di cancro?
Dove Fare il Test Genetico?
- Lo svolgimento dei test genetici può avvenire all’interno dell’ospedale in cui si trova l’unità operativa che prescrive l’esecuzione, all’esterno in una struttura facente parte del Servizio Sanitario Nazionale(SSN) o presso un erogatore privato come ad esempio Geneticlab, Laboratorio Genoma o AltaMedica.
- Se si decide di effettuare un’analisi genetica del DNA, è sicuramente importante rivolgersi ad un centro accreditato e certificato come idoneo dalle autorità competenti. Qui ci sono i centri validati per la terapia personalizzata rispetto ad alcuni tipi di tumori: BioGate
- Qui puoi vedere quali controlli medici sono utili per prevenire molte patologie a seconda del proprio sesso e della propria età: Fondazione Umberto Veronesi
- Consulta il Servizio Nazionale di Accoglienza e Informazione in ONcologia (SION). Per rafforzare l’oncologia italiana è nata l’Alleanza Contro il Cancro di cui fanno parte gli istituti scientifici più all’avanguardia nelle ricerche genetiche sul cancro in Italia. Ecco di seguito l’elenco di alcuni centri di riferimento:
- Centro di Riferimento Oncologico – Aviano
- Ist. Naz.le Tumori Regina Elena – Roma
- Fond. IRCCS Ist. Naz.le dei Tumori – Milano
- IRCSS San Martino Ist – Genova
- Ist. Naz.le T. Fondazione Pascale – Napoli
- IRCSS Giovanni Paolo II – Bari
1. Cancro al Seno e all’Ovaio
- Consulta il sito della Fondazione Umberto Veronesi
- Le più note mutazioni genetiche che predispongono a questo tipo di tumore sono quelle a carico dei geni oncosoppressori BRCA-1 e BRCA-2, da cui dipende il 50% circa delle forme ereditarie di cancro del seno.
- È stato infatti dimostrato che chi ha una madre o una sorella con questa patologia, soprattutto se contratta in giovane età, corre un rischio maggiore di svilupparla nel corso della vita rispetto a chi non ha mai avuto casi di tumore del seno in famiglia
- È importante sottolineare che avere ereditato la mutazione non significa essere certi di contrarre prima o poi la malattia, piuttosto equivale ad avere un rischio più elevato rispetto a chi non ha la mutazione. Il test genetico non è dunque uno strumento di prevenzione nel senso classico del termine, ma si limita a fornire informazioni sul rischio di ammalarsi di tumore nel corso della vita e deve essere svolto solo in caso di reale necessità, dopo una consulenza con il genetista medico.
- Occorre rivolgersi a un medico specialista: se la donna in questione rientra in una certa tipologia di rischio, si procede con il test. La Società italiana di genetica umana, che a sua volta ha recepito alcune indicazioni americane, individua l’opportunità di sottoporre a questi esami genetici solo chi ha in famiglia situazioni particolari di casi multipli (di solito in età relativamente giovane) almeno di cancro all’ovaio, da ciascuno (o uno solo) dei due rami, dunque o da parte materna o da parte paterna.
2. Fibrosi Cistica
- Consulta il sito Fondazione Ricerca Fibrosi Cistica – Onlus
- Oggi è possibile riconoscere i portatori sani con il test genetico del portatore,
eseguito in laboratori specializzati in tecniche di genetica molecolare, su presentazione di richiesta del medico curante, con il test per l’Analisi delle mutazioni del gene CFTR. - Chi è parente diretto di un malato FC ha maggiore probabilità rispetto ad altri di avere nel proprio DNA una mutazione del gene CFTR. Questo perché potrebbe aver ereditato la mutazione genetica “familiare”.
- Chi non ha casi di FC in famiglia ha comunque una probabilità su 25 circa di essere un portatore sano di fibrosi cistica. Per questa ragione è opportuno che il test sia fatto dal parente del malato ma anche dal suo partner, se c’è.
- Un elenco di centri qualificati dove è possibile avere il colloquio e il test genetico si trova nelle pagine finali del documento “Il test per il portatore sano di fibrosi cistica“.
3. Alzheimer
- Consulta il sito del Centro Alzheimer
- Le mutazioni finora identificate nella malattia di Alzheimer familiare riguardano geni chiamati presenilina-1 (PSEN1), presenilina-2 (PSEN2) e proteina precursore di beta-amiloide (APP).
- È possibile verificare la presenza di una mutazione genetica attraverso un prelievo di sangue, sul quale vengono eseguiti specifici esami di laboratorio. Queste analisi devono essere effettuate all’interno di un percorso conoscitivo strutturato detto consulenza genetica.
4. Parkinson
- Consulta il sito della Fondazione Grigioni
- Numerosi studi sugli aspetti genetici stanno cominciando a identificare i vari geni coinvolti nella predisposizione alla Malattia di Parkinson, ma attualmente, a parte rari casi, non si può stabilire con chiarezza quale è la probabilità di aver ereditato questa predisposizione all’interno della famiglia. Le rare eccezioni sono quelle famiglie in cui la predisposizione genetica è legata ad una mutazione su un singolo gene (malattia monogenica).
- I geni individuati in queste famiglie fino ad ora sono 11 (denominati PARK-1 , PARK-11) di cui 6 sono stati effettivamente identificati: alfa-sinucleina (PARK-1), parkina (PARK-2), ubiquitina idrolasi (PARK-5), PINK1 (PARK6), DJ-1 (PARK-7), LRRK2 (PARK8).
- Comunque il rischio di sviluppare la malattia nei familiari di 1° grado è basso. Il rischio relativo è circa 3; in altre parole se il rischio della popolazione generale di ammalarsi di Parkinson sopra i 65 anni di età è dell’1%, per i familiari di 1° grado di un malato di Parkinson il rischio di ammalarsi è il 3%.
5. Sclerosi Laterale Amiotrofica
- Consulta il sito dell’Associazione Sclerosi Laterale Amiotrofica Onlus
- Un difetto presente sul cromosoma 21, che codifica per un enzima, la superossido dismutasi, è associato a circa il 40% dei casi familiari di SLA, o circa il 2% dei casi di SLA globali. Il gene che presenta tali mutazioni è chiamato SOD1 e sono conosciute numerose mutazioni che possono alterare la normale funzione di tale gene.
- Per quanto riguarda l’applicazione clinica di queste conoscenze, va sottolineato come, date le implicazioni etiche e psicologiche, la complessità delle variabili ed il grosso numero di interrogativi tuttora irrisolti, il test genetico (ricerca di una possibile mutazione causale nall’ammalato o “pre-sintomatica” nei familiari sani) è consigliabile solo a malati con chiara familarità, ed eventualmente – se lo desiderano – ai parenti adulti consanguinei di primo grado dell’ammalato.
Il Verdetto Finale
La medicina di precisione ci può fornire delle cure altamente personalizzate e cucite su misura per le nostre esigenze di salute. Sebbene si stiano facendo dei passi da gigante nella ricerca medica e in quella genetica in modo particolare, bisogna fare attenzione a non svendere i nostri dati ad agenzie poco competenti. Per quanto il nostro DNA contenga informazioni preziose per poter fare la giusta prevenzione e mantenerci in salute, non è mai un destino certo ed inevitabile! Il consulto con un genetista è fondamentale per decidere se, e quando, sottoporsi ad un trattamento preventivo.